Neurologijos seminarai ISSN ISSN 1392-3064 / eISSN 2424-5917
2024, 28(102), pp. 255–272 DOI: https://doi.org/10.15388/NS.2024.28.102.8
Apžvalginis mokslinis straipsnis / Review Article
Eglė Sakalauskaitė-Juodeikienė*
Vilniaus universiteto Medicinos fakulteto Klinikinės medicinos instituto Neurologijos ir neurochirurgijos klinika
VUL Santaros klinikų Neurologijos centras
Vilniaus miesto psichikos sveikatos centras
Algis Jaraminas
Vilniaus miesto psichikos sveikatos centras
Santrauka. Dar senovėje buvo suprasta, kad poilsis ir miegas yra gyvybiškai svarbūs, tokie pat reikšmingi kaip kvėpavimas, valgymas ir kitos organizmo funkcijos. Tačiau tik paskutiniais dešimtmečiais mokslas įrodė, jog miegas – tai aktyvus procesas, kurio metu vyksta neuroninių tinklų stabilizacija, atnaujinami smegenų ir viso organizmo energiniai rezervai, reguliuojamos imuninės reakcijos, skatinama makromolekulių sintezė ir taisyklingas baltymų struktūrų susidarymas, apribojama oksidacinio streso sukelta ląstelių pažaida, vyksta informacijos perdirbimas, atranka, ilgalaikis išsaugojimas, emocijų reguliacija, toksinių metabolitų ir baltymų irimo produktų šalinimas. Psichikos ir miego sutrikimų atveju minėti procesai yra sutrikdomi. Šio apžvalginio straipsnio tikslas – išanalizuoti miego ir psichikos sutrikimų tarpusavio ryšį, atkreipiant dėmesį į skirtingas psichikos sutrikimų grupes. Straipsnyje aptariamas miego ir psichikos sutrikimų komorbidiškumas, pateikiami galimi miego ir psichikos sutrikimų atkryčių mechanizmai, charakterizuojami esminiai psichikos sutrikimams būdingi miego architektūros pokyčiai. Greta apžvelgiamos dažniau naudojamų psichotropinių vaistų poveikio miegui ypatybės, terapiniai jų skyrimo aspektai, pateikiamos kompleksinės psichoterapinio ir medikamentinio gydymo strategijos, galinčios padėti optimizuoti tiek psichikos, tiek miego sutrikimų gydymą.
Raktažodžiai: psichikos sutrikimai, miego sutrikimai, polisomnografija, psichoterapija, medikamentai.
Summary. Even in ancient times, it was understood that rest and sleep are vital processes, as essential as breathing, eating, and other bodily functions. However, only in recent decades science has demonstrated that sleep is an active process involving neuronal network stabilization, restoration of brain and whole-body energy reserves, proper protein structure formation, promotion of macromolecule synthesis, processing and long-term retention of information, emotional regulation, reduction of oxidative stress-induced cellular damage, regulation of immune responses, and the clearance of toxic metabolites and protein degradation products. In cases of mental and sleep disorders, these processes are disrupted. The aim of this review article is to analyze the relationship between sleep and mental disorders, while focusing on different groups of psychiatric conditions. We also discuss the comorbidity of sleep and mental disorders, explore how sleep disturbances may trigger relapses or worsen psychiatric symptoms, and characterize core changes in sleep architecture for various mental disorders. Additionally, we review the effects of psychotropic medications on sleep, therapeutic considerations for their usage, and present combined psychotherapeutic and pharmacological treatment strategies that can optimize the treatment outcomes for both sleep and mental disorders.
Keywords: mental disorders, sleep disorders, polysomnography, psychotherapy, medications.
________
* Address: Eglė Sakalauskaitė-Juodeikienė, Vilniaus universiteto Medicinos fakulteto Klinikinės medicinos instituto Neurologijos ir neurochirurgijos klinika, Santariškių g. 2, LT-08661 Vilnius. Tel. +370 5 236 5220, el. paštas egle.sakalauskaite-juodeikiene@mf.vu.lt
Received: 01/06/2025. Accepted: 05/07/2025
Copyright © Eglė Sakalauskaitė-Juodeikienė, Algis Jaraminas, 2024. Published by Vilnius University Press.This is an Open Access article distributed under the terms of the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited.
Jau senovėje buvo suprasta, kad miegas yra gyvybiškai svarbus, toks pat reikšmingas kaip kvėpavimas, valgymas ir kitos organizmo funkcijos. Tačiau tik paskutiniais dešimtmečiais įrodyta, jog miegas – ne pasyvus, o aktyvus procesas, kurio metu vyksta neuroninių tinklų stabilizacija, atnaujinami smegenų ir viso organizmo energiniai rezervai, reguliuojamos imuninės reakcijos, skatinama makromolekulių sintezė ir taisyklingas baltymų struktūrų susidarymas, ribojama oksidacinio streso sukelta ląstelių pažaida, vyksta informacijos perdirbimas, atranka bei išsaugojimas [1]. Miegas atlieka gyvybiškai svarbų neuroprotekcinį vaidmenį, per glimfatinę sistemą pašalindamas toksiškus metabolitus, kuriuos gamina smegenys būdravimo metu. Nustatyta, kad atminties konsolidacija vyksta tiek NREM (angl. non-rapid eye movement, lėtų akių judesių arba lėtojo), tiek REM (angl. rapid eye movement, greitų akių judesių arba paradoksinio) miego metu. Esant miego trūkumui, ypač NREM N3 (gilaus, delta miego) stokai, labiausiai nukenčia kaktinės skilties prefrontalinė žievė, atsakinga už motyvaciją, elgesį, kalbos sklandumą, mąstymą, planavimą bei impulsų kontrolę [2]. Esant bendrai miego stokai ir nepakankamam REM miego kiekiui, sutrinka emocijų ir nuotaikos reguliacija. REM miego bei sapnų metu reguliuojami, modifikuojami, pamirštami nemalonūs prisiminimai; pasak biologo ir neuromokslininko Franciso Cricko (1916–2004) ir jo kolegų, „REM fazės metu mes miegame, kad pamirštume“ [3]. Kitos sapnų funkcijų teorijos aiškina, kad sapnai atlieka epizodinės atminties konsolidavimo bei integravimo į senesnius prisiminimus funkciją [4], lemia ilgalaikę asmens adaptaciją prie psichotraumuojančių įvykių [5], pagerina asmens funkcionavimą bei emocijų reguliavimą būdravimo metu [6], palaiko asmens psichologinį indentitetą [7]. Kita vertus, skeptiškai vertinantieji šias teorijas priduria, kad sapnai gali būti tikrai REM miego epifenomenas [8]. Sigmundo Freudo (1856–1939) psichoanalitiniai miego ir sapnų procesų aiškinimai šiandien turi istorinę reikšmę [2].
Nustatyta, kad ūmus ir lėtinis miego trūkumas blogina asmens gyvenimo kokybę, darbingumą, kelia grėsmę tiek žmogaus, tiek visos visuomenės fizinei ir psichinei sveikatai. Jau prieš šimtmetį atliktais eksperimentais buvo nustatyta, kad kelių savaičių miego trūkumas laboratoriniams gyvūnams sukeldavo termoreguliacijos ir metabolizmo sutrikimus, padidėjusį apetitą, padidindavo susirgimo infekcinėmis ligomis riziką, galiausiai – lemdavo išsekimą bei mirtį. Naujesnių tyrimų duomenimis, dalinė miego deprivacija (< 5 val. per naktį) buvo susijusi su 12 proc. didesne bendra mirtingumo rizika, miego deprivaciją patiriančius asmenis lyginant su asmenimis, kurie miegodavo po 6–8 val. per naktį. Miego trūkumas yra susijęs su padidėjusia nutukimo, sumažėjusios gliukozės tolerancijos, II tipo cukrinio diabeto, širdies ir kraujagyslių, infekcinių bei kitų ligų rizika [9].
<Šio apžvalginio straipsnio tikslas – išanalizuoti miego ir psichikos sutrikimų tarpusavio ryšį, atkreipiant dėmesį į skirtingas psichikos sutrikimų grupes. Straipsnyje aptariamas miego ir psichikos sutrikimų komorbidiškumas, pateikiami galimi miego ir psichikos sutrikimų atkryčių mechanizmai, charakterizuojami esminiai psichikos sutrikimams būdingi miego architektūros pokyčiai. Greta apžvelgiamos dažniau naudojamų psichotropinių vaistų poveikio miegui ypatybės, terapiniai jų skyrimo aspektai, pateikiamos kompleksinės psichoterapinio ir medikamentinio gydymo strategijos, galinčios padėti optimizuoti tiek psichikos, tiek miego sutrikimų gydymą.
Miego trūkumas dėl prefrontalinės žievės disfunkcijos ir emocijų reguliavimo sutrikimo ne tik sukelia mieguistumą, nuovargį, blogina nuotaiką, padidina nerimą, bet ir sumažina paciento gebėjimą susitvarkyti su iškylančiais kasdieniais sunkumais. Miego trūkumas, besitęsiantis 24–48 val., sukelia suvokimo sutrikimus (iliuzijas, haliucinacijas), nerimą, dirglumą, depersonalizaciją ir dezorientaciją, mąstymo, impulsų kontrolės sutrikimus. Miego trūkumas, besitęsiantis 72 val. ir ilgiau, sukelia ūminei psichozei ir delyrui būdingą simptomatiką su regos (90 proc.), somatosensorinėmis (52 proc.) ir klausos (33 proc.) haliucinacijomis [10].
Nemiga įvairiuose epidemiologiniuose tyrimuose buvo vertinta kaip nepriklausomas rizikos veiksnys vėlesnio depresijos epizodo išsivystymui pirmąkart gyvenime. Prieš išsivystant pirmam psichozės epizodui, ligonį dažniausiai pradeda kankinti naujai atsiradę miego sutrikimai (kurių dažniausias yra nemiga). Miego sutrikimai gali indikuoti ir būsimą jau diagnozuotos psichikos ligos (pvz., šizofrenijos) paūmėjimą. Negydoma nemiga epidemiologiniuose tyrimuose buvo vertinama kaip psichikos ligas sukeliantis ir sunkinantis veiksnys [11].
Cirkadinio ritmo sutrikimai – tai neatitikimas tarp paciento miego įpročių ir normalaus, įprastinio miego modelio, atsižvelgiant į paros laiką. Cirkadinio ritmo sutrikimai sukelia nemigą nakties metu, padidėjusį mieguistumą dieną, neigiamai veikia darbingumo lygį, blogina gyvenimo kokybę. Chronotipas – tai cirkadinio ritmo elgesio pasireiškimas, asmens polinkis miegoti tam tikru metu per 24 valandas. Chronotipai skirstomi į rytinį, vakarinį bei tarpinį (kurį turi didžioji dalis, apie 60 proc., populiacijos) [12]. Vakarinis chronotipas, ypač būdingas paaugliams ir jauniems suaugusiesiems, yra siejamas su neigiama įtaka sveikatai bei socialiniam gyvenimui, sutrumpėjusia gyvenimo trukme, padidėjusiu sergamumu psichikos ir somatinėmis ligomis, padidėjusia narkotinių medžiagų vartojimo rizika. Įvairių tyrimų duomenimis, apie 25 proc. nemigos kamuojamų pacientų priskiriami vakariniam chronotipui [11]. Cirkadinio ritmo sutrikimai gali nulemti ir psichikos ligų išsivystymą. Asmenims, kelerius metus dirbantiems pamaininį darbą, padidėja depresijos išsivystymo rizika. Laiko juostų pakeitimas (angl. jet-lag) yra susijęs su padidėjusiu nerimo lygiu, disforine nuotaika, gali būti šizofrenijos ar šizoafektinio sutrikimo paūmėjimo rizikos veiksnys [13]. Sezoniniai svyravimai, metų laikų kaita taip pat gali sukelti cirkadinių procesų bei psichikos sutrikimus. Nustatyta, kad įvykdytų ir ketintų įvykdyti savižudybių skaičius įvairiose populiacijose didžiausias būna pavasarį ir ankstyvą vasarą [14].
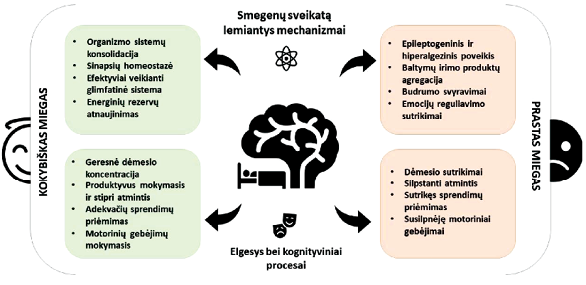
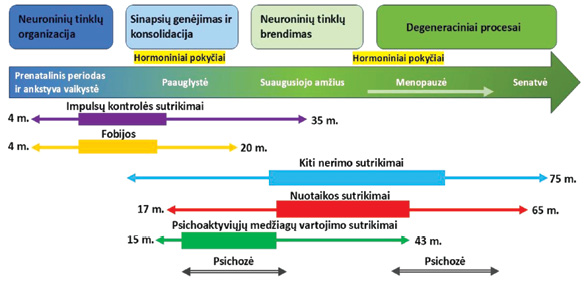
Miego kokybės, elgesio ir kognityvinių procesų sąsajos pavaizduotos 1 pav. Miego ir psichikos sutrikimų išsivystymo sąsajos ir dėsningumai įvairiose amžiaus grupėse [15] pavaizduoti 2 pav. Su miegu susijusių simptomų, būdingų tam tikriems psichikos sutrikimams, dėsningumai nurodyti 1 lentelėje. Verta pažymėti, kad joks miego sutrikimas nėra specifiškas kuriam nors psichikos sutrikimui [11].

Nuotaikos (afektiniams) sutrikimams priskiriama depresija, bipolinis afektinis sutrikimas ir kiti. Depresijos ir bipolinio afektinio sutrikimo paplitimas atitinkamai siekia 6,9 proc. ir 0,9 proc. per metus [16]. Depresija laikoma viena pagrindinių neįgalumo priežasčių pasaulyje. Naujausiais genetiniais dvynių konkordantiškumo tyrimais nustatyta, kad depresijos paveldimumas siekia 37 proc., o bipolinio afektinio sutrikimo – net iki 75 proc. [17]. Nuotaikos sutrikimai dažniausiai pasireiškia kartu su šiais miego sutrikimais: lėtine nemiga, hipersomnija, cirkadinio ritmo sutrikimais, košmariškais sapnais, neramių kojų sindromu (NKS) ir miego apnėja [18].
|
Su miegu susiję simptomai ir miego sutrikimai |
Psichikos sutrikimai |
|
Sumažėjęs miego poreikis |
– Manija, hipomanija (bipolinis sutrikimas, šizoafektinis sutrikimas) |
|
Nemiga |
– Alkoholio, narkotinių medžiagų (kanapės, opioidai, psichostimuliatoriai), seduojančių medikamentų, nikotino vartojimo nutraukimas – Intoksikacija kofeinu, nikotinu, stimuliatoriais – Depresijos epizodas (depresijos sutrikimas, bipolinis sutrikimas, šizoafektinis sutrikimas) – Ūminė reakcija į stresą, potrauminio streso, nerimo sutrikimai – Lėtinis nuovargio sindromas (neurastenija) |
|
Padidėjęs mieguistumas dieną (hipersomnija) |
– Atipinis depresijos epizodas (depresijos sutrikimas, bipolinis sutrikimas, šizoafektinis sutrikimas) – Lėtinis nuovargio sindromas (neurastenija) – Premenstruacinis disforinis sindromas – Narkotinių medžiagų (psichostimuliantų) vartojimo nutraukimas |
|
Košmariški sapnai |
– Ūminė reakcija į stresą – Potrauminio streso sutrikimas |
|
Nuovargis |
– Lėtinis nuovargio sindromas (neurastenija) – Depresijos epizodas – Kofeino vartojimo nutraukimas |
Nustatyta, kad nemiga yra nepriklausomas rizikos veiksnys depresijai de novo išsivystyti. Apie 45 proc. depresija ir 24 proc. bipoliniu afektiniu sutrikimu sergančių asmenų taip pat serga lėtine nemiga [19]. Lėtinė nemiga ir dažni košmariški sapnai yra susiję su padidėjusia savižudybės rizika. Persistuojanti nemiga, kai depresija jau yra pagydyta, yra vienas iš depresijos epizodo pasikartojimo rizikos veiksnių. Nemigos sunkumas tiesiogiai koreliuoja su depresijos sunkumu, didesne ligonio funkcine negalia, blogesniu atsaku į antidepresinį gydymą, padidėjusia savižudybės rizika. Nemiga kartu su sumažėjusiu miego poreikiu dažniausiai pasireiškia prieš manijos epizodą ligoniams, kuriems nustatytas bipolinis afektinis sutrikimas [18].
Polisomnografijos (PSG) tyrimu asmenims, sergantiems depresija, dažniausiai nustatoma pailgėjusi užmigimo latencija, pailgėjęs būdravimo laikas po užmigimo, sumažėjęs NREM miego N3 fazės kiekis, sutrumpėjusi REM miego latencija, pailgėjęs bendras REM miego kiekis, padidėjęs REM tankis (greitų akių judesių dažnis REM miego metu) [20]. Pacientų, sergančių depresija, REM miegas yra fragmentuotas, nestabilus, su gausiais mikroprabudimais, dėl to REM miego metu vykstantys emocijų reguliavimo ir limbinės sistemos neuronų stabilizavimo procesai yra sutrikę. Identiški PSG pokyčiai gali būti aptinkami ir sveikiems giminaičiams, kurių artimieji serga depresija. Pacientai dažnai skundžiasi, jog sunku užmigti, miegas yra paviršutiniškas, vargina dažni, ankstyvi nubudimai (2–3 val. anksčiau nei įprasta) paryčiais, kai kurie asmenys būna įsitikinę, kad naktį visai nemiega. Sergant bipoliniu afektiniu sutrikimu, PSG tyrimais buvo nustatomas padidėjęs REM tankis, pailgėjusi REM miego latencija ir ilgesnė NREM N3 miego trukmė, kuri buvo susijusi su didesne manijos pasikartojimo tikimybe 3 mėn. laikotarpiu [18].
Didžioji dalis depresijai gydyti skirtų antidepresantų slopina REM miegą. Anksčiau buvo teigta, jog selektyvi REM miego supresija yra vienas iš galimų depresijos gydymo metodų. Įdomu pažymėti, kad visiška vienos nakties miego restrikcija taip pat turi trumpą depresijos simptomų pagerėjimo poveikį 50– 60 proc. ligonių [21]. Kita vertus, šiandien taip pat diskutuojama, kad REM miego slopinimas yra tiktai depresijos gydymo epifenomenas, nes kai kurie antidepresantai (nefazodonas, moklobemidas) pasižymi geru antidepresiniu poveikiu, tačiau nekeičia REM miego struktūros [22].
Kai kurie seduojantys antidepresantai (mirtazapinas, trazodonas) pasižymi hipnotiniu poveikiu, padidina NREM N3 miego kiekį. Įrodyta, kad gydant vien depresiją, nemigos simptomai dažnai išlieka, tačiau tuo pat metu gydant ir depresiją, ir nemigą, galima sulaukti dvigubo teigiamo atsako. Tačiau dera nepamiršti, kad pirmojo pasirinkimo gydymo metodas ir aukso standartas lėtinei nemigai (su depresija arba be jos) gydyti išlieka kognityvinė ir elgesio terapija, skirta nemigai (KET-N) [23]. Nustatyta, kad bipoliniu afektiniu sutrikimu ir lėtine nemiga sergančių ligonių psichinės ligos paūmėjimas (naujas depresijos ar manijos epizodas) per 6 mėn. buvo mažesnis tiems, kuriems nemigai gydyti buvo taikyta KET-N, nei ligoniams, kuriems nemigai gydyti buvo taikyta tik psichoedukacija (atitinkamai 14 proc. ir 42 proc.) [24]. Antidepresantai gydymo pradžioje ar jo metu miegą gali pabloginti, todėl būtina derinti individualiai pritaikytą farmakoterapiją su KET-N [25]. KET-N apima psichoedukacinius metodus, miego higieną, relaksacinę terapiją, stimulo–kontrolės terapiją, miego ribojimo ir kognityvinę terapiją. KET-N taikoma tiesiogiai dalyvaujant pacientui (ar grupei pacientų, sergančių lėtine nemiga), tačiau taip pat gali būti taikoma nuotoliniu, skaitmeniniu būdu. Įprastai KET-N trunka 4–8 sesijas ir apima 3–4 metodikas [23]. KET-N yra sėkmingai taikoma ir Lietuvoje.
Cirkadinio ritmo sutrikimai, ypač vakarinis chronotipas, yra susiję su didesne depresijos (ypač sezoninės), bipolinio afektinio sutrikimo išsivystymo rizika [18, 26]. Cirkadinės fazės paankstinimas turi trumpalaikį teigiamą antidepresinį efektą. Rekomenduojama gydymui taikyti chronoterapiją: šviesos terapiją ankstyvomis ryto valandomis (rekomenduojamos antidepresinės šviesos lempos, praturtintos mėlynu spektru, bent 10 000 lx stiprumo, terapijos trukmė – apie 30 min., šviesos šaltinis – 0,5 m atstumu nuo paciento veido, į šviesą reikėtų pažiūrėti trumpai, po 2–3 sek., šią terapiją reikėtų taikyti kasdien, iškart pabudus ryte), vakare vengti mėlyno spektro ir kitos ryškesnės šviesos, tarp 19.00 ir 21.00 val. skirti greito veikimo melatonino 2–5 mg dozę, taip pat rekomenduojama didinti pacientų fizinį aktyvumą rytais ir dienomis, rytais ir perpiet vartoti kaloringesnį, maistingesnį maistą, užsiimti aktyvesne socialine veikla, o vakarais – valgyti lengviau virškinamą maistą, laikytis kitų miego higienos rekomendacijų (žr. 2 lentelę) [27].
|
Rekomendacija |
Paaiškinimas |
|---|---|
|
1. Kiekvieną rytą kelkitės tuo pačiu metu |
Stenkitės kiekvieną vakarą eiti miegoti tuo pačiu metu, o rytais – keltis tuo pačiu metu. Reguliarus miego režimas miegą padaro efektyvesnį |
|
2. Nemiegokite dieną, jei sunkiai užmiegate naktį |
Asmenims, sunkiai užmiegantiems naktį, poguliai dieną gali kompensuoti nakties miegą, todėl jie gali mažiau norėti miego naktį ir jų problemos dėl nemigos gali paūmėti |
|
3. Venkite kofeino turinčių gėrimų |
Kava, arbata ir daugelis kitų gėrimų bei maistas, kurio sudėtyje yra kofeino ir kuris veikia kaip stimuliatorius, gali trikdyti užmigimą. Todėl turėtų būti vengiama vartoti kofeiną iki nakties miego likus 4–6 val., taip pat reikėtų mažinti kofeino turinčių gėrimų vartojimą dienos metu |
|
4. Nevartokite alkoholio |
Nors alkoholis pagreitina užmigimą, tačiau alkoholio vartojimas sutrikdo miego struktūrą. Dėl šios priežasties alkoholis nėra geras būdas siekiant visaverčio nakties miego |
|
5. Nerūkykite |
Cigaretės ir kiti nikotino turintys produktai yra stimuliatoriai, jų turėtų būti vengiama prieš miegą ir prabudus naktį |
|
6. Mankštinkitės |
Reguliari mankšta rytais arba ankstyvą popietę, fizinis aktyvumas dienos metu pagerina gilų miegą naktį. Tačiau mankšta likus 3–4 val. iki miego gali trukdyti užmigti |
|
7. Koreguokite mitybą |
Sunkus maistas vėlyvą vakarą gali trukdyti miegui. Kita vertus, lengvas užkandis arba kitas įprastas ritualas prieš miegą gali padėti užmigti |
|
8. Sukurkite ryšį tarp miegamojo patalpos ir greito užmigimo |
Siekiant sukurti ryšį tarp miegamojo patalpos ir greito užmigimo, reikėtų laikytis šių taisyklių: – lovą reikėtų naudoti tik intymiam bendravimui ir miegui; nereikėtų lovoje skaityti, valgyti, žiūrėti TV ar užsiimti kita veikla; – reikėtų gulti tik tada, kai norisi miego; – jei negalite užmigti 15–20 min., turėtumėte atsikelti iš lovos, išeiti iš miegamojo ir vėl gultis tik tada, kai užsinorite miego; – keltis kiekvieną rytą tuo pačiu metu ir vengti numigimų dieną |
|
9. Sukurkite tinkamą miegui aplinką |
– Geriau miegama kiek vėsesnėje, gerai išvėdintoje patalpoje, tačiau užmigsite greičiau, jei prieš miegą sušilsite, pavyzdžiui, nusimaudysite po šiltu dušu. Padėti užmigti gali ir naktinė kepuraitė, vilnonės kojinės – Prieš miegą rekomenduojama prigesinti šviesas, vengti ryškaus kambario, TV ar kompiuterio ekrano apšvietimo. Jei negalite prieš miegą atsisakyti kompiuterio naudojimo, pakeiskite ekrano apšvietimą: vietoj melsvų atspalvių rinkitės rusvus, rausvus, nes mėlyno spektro šviesa turi budrumą skatinantį poveikį – Jei skaitymas prieš miegą padeda atsipalaiduoti, vakare rekomenduojama rinktis lengvo turinio knygą, o ne švytintį elektroninės skaityklės ekraną – Rekomenduojama vengti triukšmo. Pavyks greičiau užmigti, jei nematysite ir negirdėsite tiksinčio laikrodžio |
|
10. Prieš miegą venkite veiklos, didinančios susijaudinimą |
Prieš miegą atsisakykite veiklos, didinančios sujaudinimą (pvz., sunkūs fiziniai pratimai, įtraukiančių knygų skaitymas, įtemptas TV žiūrėjimas, šeimos konfliktai ir kita) |
|
Prisiminkite, kad atsitiktinė nemigos naktis sveikatai nekenkia! |
|
Pusei depresija sergančių pacientų pasireiškia neramių kojų sindromo simptomai, iš kurių dalis gali būti sukeliami arba pasunkinami depresijai gydyti skiriamų medikamentų [18]. Gyvenimo būdo korekcijos priemonės (reguliarus fizinis aktyvumas, kofeino ir kitų stimuliantų vartojimo mažinimas) gali palengvinti NKS simptomus, taip pat patariama laikytis miego higienos rekomendacijų, vengti miego deprivacijos, nutraukti NKS simptomus galinčių bloginti vaistų vartojimą arba sumažinti jų dozes. Visiems pacientams, turintiems NKS simptomų, turi būti įvertinta feritino koncentracija serume ir transferino įsotinimas. Jei serumo feritino koncentracija < 50 mkg/l, o transferino įsotinimas < 20–25 proc., būtina pradėti gydymą geležies preparatais. Dėl geležies preparatų skyrimo turi būti svarstoma, net jeigu feritino koncentracija yra > 50 mkg/l, tačiau transferino įsotinimas < 20–25 proc. NKS gydymui kaip antro pasirinkimo vaistai rekomenduojami alfa-2-delta (α2δ) kalcio kanalų ligandai gabapentino enakarbilis arba pregabalinas. NKS gydymui kaip trečio pasirinkimo vaistai gali būti skiriami dopamino receptorių agonistai, tačiau jie yra susiję su augmentacijos rizika. Opioidai NKS gydymui skiriami, kai kiti būdai yra neveiksmingi.
Hipersomnija nustatoma iki 14 proc. depresija ir 30 proc. bipoliniu afektiniu sutrikimu sergančių ligonių. Padidėjęs mieguistumas dieną gali pasireikšti ir dėl jaučiamo nuovargio, anhedonijos, motyvacijos stokos, seduojančių antidepresantų vartojimo, vakarinio chronotipo ir kitų su depresija susijusių veiksnių [18].
Košmariški sapnai dažniau pasireiškia asmenims, kuriems būdingi nuotaikos sutrikimai, palyginti su sveikais kontroliniais tiriamaisiais [18].
Obstrukcinės miego apnėjos (OMA) dažnis depresija sergančių ligonių grupėje yra kiek didesnis, palyginti su sveika populiacija. Taikant CPAP (angl. continuous positive airway pressure, nuolatinio teigiamo slėgio ventiliacijos) terapiją OMA gydymui, nustatytas teigiamas poveikis žvalumo, koncentracijos, motyvacijos didinimui, atminties gerinimui – šie simptomai būdingi tiek OMA, tiek depresijai [18].
Nerimo sutrikimais sergantis ligonis patenka tarsi į užburtą ratą: baimė ir nerimas padidina budrumo lygį dieną, pacientas pradeda vengti nerimą keliančių situacijų, keičiasi jo elgesys, trinka kasdienė veikla ir miegas, nepakankamas ir nekokybiškas miegas dėl padidėjusio budrumo naktį blogina funkcionavimą dienos metu, o tai dar labiau padidina nerimo lygį. Nemigą patiria apie 33 proc. visų nerimo sutrikimais sergančių pacientų [28]. Tyrimais nustatyta, kad ligoniai, kuriems būdingi nerimo sutrikimai, turi didesnę riziką susirgti nemiga, taip pat įrodyta, kad sergantiesiems nemiga yra didesnė nerimo sutrikimų de novo išsivystymo rizika [29]. Tiriamiesiems, kurie 5 dienas miegojo po 4 val., sumažėjo funkciniai ryšiai tarp kaktinių skilčių ir migdolinio kūno (amygdala), dėl to padidėjo jų atsakas į neigiamus dirgiklius ir blogą nuotaiką [30]. Miego deprivacija sukelia ir neigiamų emocijų (pvz., baimės) apdorojimo centrinėje nervų sistemoje (CNS) sutrikimus. Įrodyta, kad REM miegas yra itin svarbus emocijų kontrolei: stiprina su emociniu įvykiu susijusią deklaratyvinę atmintį ir mažina emocinį atsaką, kurį tas įvykis sukelia. Kokybiškas REM miegas svarbus psichotraumų emociniam apdorojimui, mažina potrauminio streso sutrikimo išsivystymo riziką [31].
Asmenų, kuriems būdingi nerimo sutrikimai, PSG tyrimais nustatoma pailgėjusi miego latencija, sumažėjęs bendras miego kiekis ir miego efektyvumas, miego struktūros pokyčiai (daugiau paviršutiniško NREM N1 miego, mažiau gilaus, delta miego – NREM N3), taip pat registruojami REM miego pakitimai. Miego, kaip ir būdravimo metu, pacientas negali atsipalaiduoti, jo budrumo lygis yra padidėjęs [32].
Apie 70 proc. panikos atakas patiriančių pacientų patiria ir naktines panikos atakas, dažniausiai pasireiškiančias NREM miego N2, N3 stadijose [33]. Jas lydi stipri baimė, artėjančios grėsmės nuojauta, autonominis sujaudinimas, paskui – baimė užmigti, vengiantis elgesys. Skirtingai nei kitų NREM parasomnijų atvejais, ligoniai panikos atakas prisimena gerai. Kadangi pacientai pabunda nuo oro trūkumo jausmo, tikslinga atlikti PSG tyrimą ir naktines panikos atakas skirti nuo miego apnėjos. Svarbios miego higienos rekomendacijos, gyvenimo būdo korekcija (kofeino, nikotino, kitų stimuliantų vartojimo mažinimas dienos metu), paciento elgesio korekcija (miego deprivacijos mažinimas) [28].
Potrauminio streso sutrikimui būdingi atsikartojantys, su traumuojančiu įvykiu susiję košmariški sapnai ir nemiga, kurie įeina ir į šio sutrikimo diagnostinius kriterijus. Šiai pacientų grupei taip pat gali pasireikšti REM parasomnija. PSG tyrimais nustatomi šie pakitimai: pailgėjusi užmigimo latencija, dažnesni prabudimai, ilgesnė NREM N1 miego trukmė, trumpesnė N3 miego trukmė, padidėjęs REM tankis [20]. Nustatyta, kad REM miego nestabilumas po įvykusio trauminio įvykio yra susijęs su didesne potrauminio streso sutrikimo išsivystymo rizika [34]. REM miego elgesio sutrikimas (REM miegas be atonijos, motorinė sapno realizacija) taip pat gali pasireikšti potrauminio streso sutrikimu sergantiems asmenims veikiau dėl padidėjusio budrumo lygio ir raumenų aktyvumo miego metu, bet ne dėl prasidėjusios neurodegeneracijos.
Nemiga ir generalizuotas nerimo sutrikimas yra susiję kaip komorbidinės lìgos dėl anksčiau išvardytų priežasčių: padidėjusio budrumo lygio, sutrikusių funkcinių ryšių tarp kaktinių skilčių ir midgolinio kūno bei kitų procesų. Ligoniai, sergantys fobiniais nerimo sutrikimais, dažniausiai serga ir lėtine nemiga [28].
Obsesinis kompulsinis sutrikimas yra susijęs su sumažėjusia bendra miego trukme, miego struktūros pokyčiais (PSG registruojama daugiau paviršutiniško miego, mažiau gilaus, NREM N3 miego) [28].
Gydant miego sutrikimus, efektyvesnis tampa ir nerimo sutrikimų gydymas. Gydant nerimo sutrikimus pabrėžiama psichologinių intervencijų svarba, o tai yra puiki galimybė kartu taikyti KET-N (pirmo pasirinkimo metodas lėtinei nemigai gydyti) su įprasta KET (nerimo simptomų valdymui), prireikus – skirti medikamentus (benzodiazepinai, jų receptorių agonistai gali būti skiriami trumpalaikiam nemigos gydymui) optimaliausiam rezultatui pasiekti [35].
Plačiausiai vartojamos nereceptinės ir legalios medžiagos, veikiančios miegą, yra alkoholis, nikotinas ir kofeinas. Sirgdami miego sutrikimais, pacientai gali savavališkai, savigydos tikslais, pradėti vartoti įvairias medžiagas. Kita vertus, šias ir kitas medžiagas vartojantiems asmenims gali naujai pasireikšti arba paūmėti jau diagnozuoti miego ir psichikos sutrikimai. Rekomenduojama šias ir kitas narkotines medžiagas vartojančius asmenis tirti dėl psichikos sutrikimų, nemigos, miego apnėjos sindromo, neramių kojų sindromo ir periodinių galūnių judesių sutrikimo miego metu (PGJM), o juos nustačius – pradėti gydyti [36].
Alkoholio vartojimo paplitimas bendrojoje populiacijoje siekia 65 proc., apie 4 proc. asmenų yra priklausomi nuo alkoholio [37]. Alkoholio vartojimas dvigubai dažniau pasitaiko tarp sergančiųjų paplitusiais psichikos (nuotaikos, nerimo) sutrikimais. Psichikos sutrikimo pradžia dažniau būna ankstesnė nei alkoholio vartojimo sutrikimų, o tai gali turėti praktinę reikšmę sudarant miego sutrikimų gydymo planą. Ūminė intoksikacija alkoholiu padidina CNS slopinimą per gama amino sviesto rūgšties A tipo (GABAA) receptorius: sutrumpėja užmigimo latencija, padidėja NREM miego kiekis pirmoje nakties pusėje. Taigi alkoholis nemiga sergantiems asmenims gali iš pradžių pasirodyti kaip efektyvi priemonė nemigos simptomams kontroliuoti. Tačiau, vartojant alkoholį, ilgainiui sutrikdomas miegas antroje nakties pusėje, pažeidžiama REM miego fazių struktūra, dažnėja nubudimai, trumpėja bendras miego kiekis, pasireiškia nerimas ryte, pasunkėja nemigos simptomai [38]. Nustatyta, kad nemiga sergančių asmenų, vartojančių alkoholį, savižudybės rizika yra gerokai didesnė, palyginti su alkoholio nevartojančiais asmenimis [39]. Manoma, kad asmenims, sergantiems nemiga ir priklausomiems nuo alkoholio, reikia vienu metu gydyti abi ligas: taikyti KET-N nemigai gydyti ir kartu gydyti priklausomybę. Kadangi alkoholis atpalaiduoja viršutinių kvėpavimo takų raumenis ir slopina CNS kvėpavimo centrus, sergant miego apnėja ir pavartojus alkoholio, apnėjų skaičius nakties metu padidėja. Alkoholis taip pat yra NKS ir PGJM rizikos veiksnys [36].
Kanapių produktų vartojimas dėl jų legalizavimo kai kuriose šalyse pastaraisiais metais išaugo nuo 4 iki 9,5 proc. [40]. Tetrahidrokanabinolis (THK) iš daugiau nei 100 kanapėse esančių junginių pasižymi stipriausiomis psichoaktyviosiomis savybėmis. Nors THK vartojimas susijęs su sutrumpėjusia miego latencija, THK trumpina REM miego kiekį, blogina prisiminimų konsolidaciją, ilgainiui vystosi tolerancija. Dėl lėtos THK eliminacijos seduojantis šio narkotiko efektas jaučiamas ir kitą dieną – padidėja mieguistumas. THK vartojimo nutraukimo simptomams būdingas nerimas, ryškūs sapnai, nemiga, prakaitavimas, dirglumas [36].
Europos populiacijoje didelės rizikos opioidų vartojimas tarp suaugusiųjų siekia 0,4 proc. [41]. Pastebėta, kad pastaruoju metu Vakarų pasaulyje išaugo metadono, fentanilio, morfino, kodeino, tramadolio ir oksikodono vartojimas medicinoje. Kaip nelegalus opioidas Lietuvoje šiuo metu labiausiai yra paplitęs karfentanilis. Narkotikų, tabako ir alkoholio kontrolės departamento (NTAKD) duomenimis, heroino vartojimas šiuo metu dažniau pasitaiko ne Lietuvoje, o kitose pasaulio šalyse [42]. Opioidai jungiasi prie CNS opioidinių receptorių, sukelia analgeziją, pailgina užmigimo latenciją bei REM miego latenciją, sumažina miego efektyvumą ir bendrą miego kiekį, miegas tampa fragmentuotas. Opioidai pablogina kvėpavimą nakties miego metu [43], padidina centrinių miego apnėjų kiekį. Opioidai didina mirtingumą nuo širdies ir kraujagyslių ligų, nutraukus – sukelia NKS paūmėjimą.
Priklausomybė nuo kokaino vartojimo pasaulyje siekia 0,1 proc. [44]. Kokainas blokuoja presinapsinius dopamino transporterius n. accumbens ir prefrontalinės žievės srityse, padidindamas aktyvinantį dopamino poveikį CNS. Vartojantiems kokainą sumažėja subjektyvus miego poreikis, pailgėja užmigimo latencija, sumažėja miego efektyvumas, bendras miego kiekis, pailgėja būdravimo laikas po užmigimo, t. y. vystosi lėtinės nemigos simptomai [36].
Psichostimuliantus (amfetaminą, metamfetaminą ir kitus) bent kartą per gyvenimą yra pabandę 3,7–4,1 proc. Europos gyventojų [41]. Amfetaminai slopina dopamino, noradrenalino ir serotonino atgalinį grąžinimą sinapsėse, didina budrumą, pailgina užmigimo latenciją, sumažina bendrą miego kiekį, miego efektyvumą, sumažina tiek NREM, tiek REM miego kiekį [45], padidina apnėjų ir hipopnėjų kiekį miego metu. Kofeinas sumažina NREM N3 miego kiekį.
Haliucinogenų (liserginės rūgšties dietilamido (LSD), psilocibino, haliucinogeninių grybų) vartojimas Europos populiacijoje siekia < 1,5 proc. [41]. Haliucinogenai pailgina užmigimo latenciją, sutrikdo nakties miego struktūrą, sumažina REM miego kiekį [46].
Pasaulyje kasdien rūkantys nurodo iki 25 proc. vyrų ir 5,4 proc. moterų [47]. Nikotinas stimuliuoja cholinerginę sistemą CNS, netiesiogiai veikia gliutaminerginę, dopaminerginę, serotoninerginę sistemą. Nikotinas didina budrumą, pailgina užmigimo latenciją bei būdravimo laiką po užmigimo, sumažina NREM ir REM miego kiekį, padidina oksidacinio streso sukeliamą pažaidą, pasunkina OMA simptomus, padidina mirtingumą nuo širdies ir kraujagyslių ligų, naujai sukelia arba pasunkina jau esančių NKS ir PGJM simptomus [36].
Lietuvoje dėl įvairių priklausomybės ligų gydymo galima kreiptis į Respublikinio priklausomybės ligų centro filialus, kur teikiama psichologinė intervencija ir konsultavimas, medikamentinis gydymas ir psichosocialinė pagalba. Metantiesiems rūkyti taip pat galima kreiptis į miestų visuomenės sveikatos biurus.
Šizofrenijos spektro sutrikimai apima šizofreniją, šizoafektinį sutrikimą ir kliedesinį sutrikimą. Šizofrenijos paplitimas siekia 4/1000 asmenų, ši liga pasaulyje užima 15 vietą pagal ligos sukeliamą naštą [48]. Daugiau nei prieš 100 m. Emilis Kraepelinas (1856–1926) nurodė, kad nemiga ir košmariški sapnai yra vieni būdingiausių miego sutrikimų dementia praecox sergantiems asmenims [49]. Vėliau buvo pastebėta, kad fenomenologiniu požiūriu psichiškai sveikų asmenų sapnai savo turiniu yra panašūs į psichozes, patiriamas būdraujant. Tuo remiantis, buvo iškelta viena iš šizofreniją aiškinančių hipotezių, kuri bandė pagrįsti šizofreniją kaip REM miego sutrikimą (REM miego ir sapnų epizodai, įsiterpiantys į būdravimą) [50]. Tačiau ši hipotezė, atlikus PSG tyrimus, nepasitvirtino.
Ilgą laiką miego sutrikimai šizofrenija sergantiems asmenims buvo vertinami kaip psichozės epizodo padarinys arba epifenomenas (nespecifinis psichologinį stresą nurodantis žymuo). Tačiau pastaraisiais metais nustatyta, kad miego sutrikimai yra vieni iš psichozės epizodo pasireiškimą lemiančių veiksnių [51]. Įrodyta, kad būtina gydyti ne tik psichozę, bet ir miego sutrikimą – gydant miego sutrikimą, lengvėja psichozės simptomai. OASIS tyrime (2017 m.) buvo įrodyta, kad, šizofrenija sergantiems asmenims taikant KET-N kartu pasireiškiančios nemigos gydymui, sumažėja paranoja, haliucinacijų dažnumas ir sunkumas [52]. Nustatyta, kad vaiksytėje patiriami košmariški sapnai yra susiję su padidėjusia psichozės išsivystymo rizika 12 ir 18 m. amžiuje galbūt dėl šias dvi ligas siejančių tų pačių poligeninių etiologinių veiksnių [53].
Sergant šizofrenija, PSG tyrimu dažniausiai nustatomas sutrumpėjęs bendras miego laikas, pailgėjusi užmigimo latencija, pailgėjęs būdravimo laikas po užmigimo, sumažėjęs miego efektyvumas, sutrumpėjusi NREM ir REM miego trukmė [54].
Nemigos simptomai, kuriuos patiria maždaug pusė visų šizofrenija sergančių pacientų, dažniausiai nurodo būsimą šizofrenijos paūmėjimą. Nemiga šių ligonių grupėje taip pat gali išsivystyti dėl psichozės sukelto padidėjusio budrumo lygio, cirkadinio ritmo sutrikimo (vėluojančios melatonino sekrecijos), dažnų numigimų dienos metu (pvz., bandant užmigti ir taip atsiriboti nuo girdimų balsų), psichinės ligos neįgalumo nulemto hipodinamiško gyvenimo būdo ir kitų veiksnių [51]. Įrodyta, kad, be tinkamai parinktų vaistų, nemigai gydyti veiksminga KET-N, kurią galima taikyti pagal specialų protokolą: 9 individualias sesijas per 2 savaites dar hospitalizacijos psichikos sveikatos centre metu [55].
Šizofrenija sergantiems asmenims taip pat būdingi košmariški sapnai, juos patiria apie pusė visų ligonių. Košmariški sapnai dažniausiai būna susiję su dienos metu patiriama psichopatologija, kuri vėliau atsikartoja naktį sapnuojant. Košmariškų sapnų gydymui rekomenduojama taikyti 4 sav. trukmės individualią psichoterapiją, susidedančią iš psichoedukacijos (ligoniui paaiškinama apie REM miego funkcijas, košmariškų sapnų priežastis) bei vaizdinių atkūrimo terapijos (angl. imagery rehearsal therapy), kai vaizuotėje būdravimo metu atkuriamas sapnuojamas košmaras, sukuriama gera jo pabaiga, mokomasi valdyti sapno turinį ir baigtį [51].
Miego apnėja, palyginti su sveika populiacija, kiek dažniau pasitaiko šizofrenija sergančių asmenų grupėje, nes jie dėl vartojamų antipsichotikų nepageidaujamo poveikio yra labiau linkę tukti, taip pat dažnai yra nedarbingi ir mažiau juda. Nustatytas teigiamas CPAP terapijos poveikis miego apnėjos gydymui ir svorio kontrolei [51].
Neramių kojų sindromas nustatomas penktadaliui visų šizofrenija sergančių asmenų. Antipsichotikai gali pasunkinti NKS simptomus [51]. Visiems pacientams, turintiems NKS simptomų, turi būti įvertinta feritino koncentracija serume, taip pat transferino įsotinimas, ir svarstoma dėl pirmos eilės gydymo geležies preparatais.
Hipersomnija gali būti sukeliama tiek cirkadinio ritmo sutrikimų (šizofrenija sergančių asmenų chronotipas dažniausiai yra vakarinis), tiek paciento elgesio (miegas dienos metu tampa savotišku pabėgimu nuo varginančių psichozės simptomų), tiek šizofrenijai gydyti skirtų vaistų [56]. Klozapinas yra vienas stipriausių seduojančių antipsichotikų – sutrumpina užmigimo latenciją, didina bendrą miego kiekį, miego efektyvumą, NREM miego kiekį, gali sukelti mieguistumą dienos metu. Detaliau apie antipsichotikų poveikį miegui žr. 3 lentelėje.
|
Vaistų grupės ir pagrindiniai atstovai |
Poveikis miegui ir PSG |
Nepageidaujamas poveikis |
Kiti klinikiniai |
|---|---|---|---|
|
SSRI: escitalopramas, fuoksetinas, sertralinas, citalopramas, paroksetinas, fluvoksaminas |
Pailgėjusi užmigimo latencija, |
Sunku užmigti, miegas paviršutiniškas, prastesnės kokybės, dažni nubudimai; gali provokuoti NKS, PGJM |
Įprastai skiriami ryte. Poveikis nevienalypis: labiau aktyvuoja fluoksetinas; (es)citalopramas nemigą sukelia rečiau; fluvoksaminas ir paroksetinas dėl anticholinerginio ir antihistamininio poveikio gali sukelti mieguistumą – kartais gali būti skiriami vakare arba paros dozę padalinus į dvi dalis |
|
SNRI: venlafaksinas, duloksetinas, desvenlafaksinas |
Panašus į SSRI |
Panašus į SSRI, bet pasižymi ir ryškiais sapnais, košmarais; gali provokuoti NKS, PGJM |
Įprastai skiriami ryte. Dažniau sukelia nemigą, tačiau kai kuriems pacientams gali pasireikšti ir mieguistumas dieną. Depresijai gydyti duloksetinas gali būti skiriamas paros dozę padalinus į dvi dalis: ryte ir vakare |
|
TCA: klomipraminas, doksepinas, amitriptilinas, nortriptilinas |
REM miego slopinimas, NREM N3 miego ilginimas |
Antihistamininis ir anticholinerginis poveikis sukelia terapinį sedacinį efektą ir kitą nepageidaujamą poveikį; gali provokuoti NKS ir PGJM |
Stipriu sedaciniu poveikiu pasižymi klomipraminas, taip pat turi polinkį sukelti NKS; kitų TCA sedacinis poveikis išreikštas, bet nortriptilinui būdingesnis aktyvinantis poveikis |
|
MAO-I: fenelzinas, moklobemidas, tranilcipraminas |
Pailgėjusi užmigimo latencija, REM miego fragmentacija |
Dėl kliniškai reikšmingų sąveikų su vaistais ir maisto produktais naudojami retai; serotonino sindromo, hipertenzinės krizės rizika |
Lietuvoje neregistruoti. Gali būti naudingi gydant atipines ar gydymui atsparias depresijas, kai ryški somnolencija |
|
Kito veikimo antidepresantai: mirtazapinas, trazodonas, bupropionas |
Mirtazapinas ir trazodonas ilgina bendrą miego trukmę, NREM N3 miegą, ilgina REM latenciją. Bupropionas trumpina REM latenciją, ilgina REM miegą |
Mirtazapinas ir trazodonas siejami su mieguistumu dieną (dažniausiai praeinančiu), kartais – ryškiais sapnais ir košmarais, hiperhidroze naktį, gali provokuoti NKS, PGJM. Bupropionas dažniau sukelia nemigą, kartais ir ryškius sapnus |
Mirtazapinas < 30 mg dozėmis daro stiprų sedacinį poveikį, tačiau skiriant > 30 mg, persvarą įgauna noradrenerginė neurotransmisija – mieguistumas sumažėja. Bupropionas naudingas esant hipersomnijai |
|
BDZ: lorazepamas, bromazepamas, diazepamas, klonazepamas, alprazolamas, triazolamas, temazepamas |
Sutrumpėja užmigimo latencija, pailgėja bendra miego trukmė, NREM N2 miego kiekis, bet sutrumpėja NREM N3 ir REM miegas, ilgėja REM miego latencija |
Dažniausiai toleruojami ir veikia greitai, subjektyviai miego kokybė tampa geresnė, tačiau PSG miego architektūra – dezorganizuota. Ilgos pusinės eliminacijos laikotarpio vaistai sukelia mieguistumą dieną, trumpos – greitesnį pripratimą |
Reikėtų skirti trumpais kursais, iki 4 sav., nes tolerancija vystosi greitai. Kartais – tinkama alternatyva kitų psichotropinių vaistų sukeltai nemigai gydyti. Miorelaksacinis poveikis yra susijęs su padidėjusia griuvimų rizika. Vartojant ilgai – nutraukimas turi būti palaipsnis, lėtas. Būdinga rikošetinė nemiga nutraukus |
|
Z hipnotikai: zolpidemas, eszopiklonas, zopiklonas, zaleplonas |
Sutrumpėja užmigimo latencija, pailgėja NREM N3 miego trukmė, bet sutrumpėja REM miegas |
Subjektyviai miego kokybė gerėja. Miego architektūra sutrikdoma mažiau, negu vartojant BDZ. Gali pasireikšti NREM parasomnijos, kognityviniai sutrikimai dienos metu |
Reikėtų skirti trumpais kursais, iki 4 sav. Tolerancija ir priklausomybė vystosi lėčiau nei skiriant BDZ. Nereikšmingas miorelaksacinis poveikis – mažesnė griuvimų rizika |
|
Atipiniai antipsichotikai: klozapinas, olanzapinas, kvetiapinas, risperidonas, amisulpridas, aripiprazolis, kariprazinas |
Ilgėja bendras miego laikas, trumpėja užmigimo latencija, mažėja REM miego kiekis |
Kartais efektyviai gydo nemigą, tačiau dažnai sukelia reikšmingą patologinį mieguistumą dieną. Aripiprazolis ir kariprazinas dažniau sukelia nemigą |
Klozapinas pasižymi labai stipria sedacija. Olanzapino, risperidono ir kvetiapino poveikis taip pat reikšmingas. Kvetiapino iki 50 mg dozės pasižymi tik antihistamininiu poveikiu. Atsižvelgiant į sedacinį arba aktyvuojantį efektą, skiriami vartoti ryte arba vakare, taip pat paros dozė gali būti suvartojama per kelis kartus |
|
Tipiniai antipsichotikai: haloperidolis, chlorpromazinas, levomepromazinas, chlorprotiksenas, zuklopentiksolis, flupentiksolis |
Poveikiu skiriasi tarpusavyje. Ilgėja miego trukmė, trumpėja užmigimo latencija, ilgėja REM miego latencija |
Dėl mieguistumo dieną ir adrenolitinio poveikio skirti gali būti sudėtinga. Turi didesnį polinkį sukelti ekstrapiramidinius simptomus, didina NKS, PGJM riziką |
Stipriausiu sedaciniu poveikiu pasižymi chlorpromazinas ir levomepromazinas, kiek mažesniu – zuklopentiksolis. Haloperidolis gali sukelti tiek sedaciją, tiek nemigą. Flupentiksolis turi labiau aktyvinantį poveikį |
|
Nuotaikos stabilizatoriai: litis, valproatas, karmabamazepinas, lamotriginas |
Litis ilgina REM latenciją, NREM N3 miegą, ilgina bendrą miego trukmę. Valproatas ilgina bendrą miego trukmę. Karbamazepinas ilgina bendrą ir NREM N3 miego trukmę, slopina REM miegą. Lamotriginas ilgina REM miegą |
Litis, valproatas, karbamazepinas kartais sukelia mieguistumą dieną, tačiau laikui bėgant mieguistumas mažėja. Lamotrigino sedacinis poveikis menkas, kartais gali aktyvinti ir sukelti nemigą |
Skiriant šiuos vaistus ne epilepsijos, o psichikos ligų gydymui, pasireiškus perteklinei sedacijai dieną, vaisto vartojimo grafiką bei dozę galima koreguoti |
|
Stimuliatoriai: metilfenidatas, modafinilis, amfetamino druskos |
Ilgina užmigimo latenciją, trumpina miego trukmę, didina miego fragmentaciją |
Dėl aktyvinančio poveikio linkę sukelti nemigą, dažnus nubudimus naktį |
Skiriami pirmoje dienos pusėje, dienos metu pasireiškiantis aktyvinantis poveikis ilgainiui „nusidėvi“. Gydymo pradžioje nemiga gali būti ryški |
Ankstyva psichozių diagnostika ir intervencija yra esminiai veiksniai, lemiantys geresnes ilgalaikes išeitis – geresnę simptomų kontrolę, atkryčio rizikos mažinimą, geresnę gyvenimo kokybę. Atkryčių prevencijai būtina įvairiapusė prieiga, įskaitant tiek palaikomąjį medikamentinį gydymą, tiek psichosocialines intervencijas. Svarbu nedelsiant reaguoti į paciento psichikos būklės pokyčius, laiku užtikrinti pagalbą, taip gerinant asmens socialinį funkcionavimą ir mažinant hospitalizacijų poreikį [57].
Valgymo sutrikimai yra susiję ne tik su širdies ir kraujagyslių ligų komplikacijomis, sumažėjusiu kaulų tankiu, elektrolitų pusiausvyros sutrikimais, dantų emalio erozijomis, vaisingumo sutrikimais, bet ir su tokiais miego sutrikimais kaip nemiga bei cirkadinio ritmo sutrikimai. Nervinė anoreksija yra didžiausiu mirtingumu pasižyminti psichikos liga [58]. Ne tik šviesa, bet ir valgymo įpročiai yra vieni stipriausių dienos ir nakties ritmo reguliatorių: dėl nereguliaraus, kompulsinio maitinimosi trinka ligonių cirkadinis ritmas. Pacientams, kurie turi valgymo sutrikimų, yra nustatomi melatonino, oreksino, grelino, leptino išsiskyrimo sutrikimai [59].
Asmenybės sutrikimams, ypač ribinio tipo, būdingi cirkadinio ritmo sutrikimai ir košmariški sapnai. PSG tyrimais nustatyta pailgėjusi užmigimo latencija, sumažėjęs bendras miego kiekis bei miego efektyvumas, sumažėjęs NREM N3 miego kiekis ir padidėjęs REM tankis [60].
Dėmesio trūkumo ir hiperaktyvumo sutrikimas iki 70 proc. atvejų pasireiškia kartu su cirkadinio ritmo sutrikimais (vėlyvosios miego fazės sutrikimu) [61]. Iki šiol nėra aišku, ar cirkadinio ritmo sutrikimai yra psichikos ligos priežastis, simptomas, ar pasekmė. Cirkadinio ritmo sutrikimai gydomi šviesos terapija, melatoninu. Taip pat šių ligonių grupėje nustatomas padidėjęs sergamumas NKS (iki 44 proc., o bendrojoje populiacijoje NKS dažnis siekia 9–15 proc.) [62]. Neramių kojų sindromas gydomas gyvenimo būdo, žalingų įpročių korekcija, skiriami geležies preparatai pagal feritino lygį, akcentuojamos miego higienos rekomendacijos [59].
Apie 58 proc. tėvų, kurių vaikams nustatytas Aspergerio sindromas, skundžiasi vaikams pasireiškiančiais miego sutrikimais [63]. PSG tyrimais nustatyta pailgėjusi užmigimo latencija, pailgėjęs būdravimo laikas užmigus, sumažėjęs miego efektyvumas, pailgėjusi REM miego latencija, sumažėjusi bendra REM miego trukmė [20]. Tyrimais buvo nustatyti cirkadinio ritmo sutrikimai dėl melatonino sekrecijos sutrikimų. Įrodyta, kad melatonino skyrimas asmenims, kuriems diagnozuotas Aspergerio sindromas, pagerina ne tik miegą, bet ir jų elgesį [64].
Psichotropiniai vaistai turi didelę įtaką miegui ir budrumui, jų poveikis varijuoja nuo stipriai seduojančio iki aktyvinamojo (žr. 3 lentelę).
Daugeliu atvejų seduojantys vaistai (pvz., seduojantys tricikliai antidepresantai, mirtazapinas ir daugelis neuroleptikų) veikia blokuodami histaminerginius H1, serotoninerginius 5-HT2A ir kitus budrumą veikiančius receptorius. Šie preparatai paprastai sutrumpina užmigimo latenciją ir pailgina bendrą miego kiekį, o tai lengvina nemigos simptomus. Tačiau šie vaistai taip pat gali sukelti mieguistumą dieną, veikti gebėjimą vairuoti ir valdyti mechanizmus, sukelti kognityvinius sutrikimus, didinti griuvimų riziką, gydymo metu gali išsivystyti tolerancija sedaciniam vaisto poveikiui [65, 66, 67]. Aktyvinantys vaistai (pvz., SSRI – selektyvūs serotonino reabsorbcijos inhibitoriai, SNRI – serotonino ir norepinefrino reabsorbcijos inhibitoriai, bupropionas, stimuliatoriai ir kiti) veikia stiprindami specifinių monoaminų neurotransmisiją, fragmentuoja miegą, pasunkina nemigos simptomus.
Seduojantis ir aktyvinantis medikamentų poveikis turi didelę reikšmę pacientų režimo laikymuisi, bendradarbiavimui. Rytinis slopinimas ir nuovargis, negilus ir prastos kokybės miegas neigiamai veikia ligonio gyvenimo kokybę [11]. Nors mokslinėje literatūroje ir akcentuojamas siekis skirti monoterapiją, klinikinėje praktikoje pacientų psichikos sutrikimų simptomų kontrolei vaistus tenka kombinuoti (pvz., skiriant antidepresantų, neuroleptikų bei nuotaikos stabilizatorių derinius). Skiriant šias kombinacijas, būtina įvertinti kumuliacinį medikamentų poveikį simptomams, miego architektūrai ir paciento funkcionavimui dienos metu [68, 69, 70].
Dalis psichotropinių vaistų yra siejami su OMA ir PGJM atsiradimu arba pasunkėjimu. Tas pats vaistas gali būti ir naudingas, ir žalingas, turėti skirtingą poveikį miegui, tai priklauso nuo dozės ir vartojimo laiko bei trukmės [71]. Pritaikant psichotropinio vaisto vartojimo režimą ir skiriant mažiausią veiksmingą dozę, kartais galima sumažinti nepageidaujamą sedacinį poveikį dieną arba nemigą naktį. Taikydami kompleksinį gydymą, gydytojai gali pagerinti psichikos ir miego sutrikimų gydymo išeitis. Greta rekomenduojama taikyti KET-N nemigos gydymui, chronoterapiją – cirkadinio ritmo sutrikimų gydymui, skirti miego higienos rekomendacijas visiems miego sutrikimams gydyti, nes tai sumažina farmakologinės terapijos poreikį ir padeda pasiekti ilgalaikių teigiamų rezultatų [72, 73, 74, 75].
1. Vis daugiau mokslinių tyrimų nurodo abipusį miego ir psichikos sutrikimų ryšį: net ir izoliuotas miego trūkumas, trunkantis 24–48 valandas, gali būti pakankamas sukelti pažinimo, suvokimo, emocijų reguliacijos, impulsų kontrolės sutrikimus; negydoma nemiga yra psichikos sutrikimų atsiradimo ir paūmėjimo rizikos veiksnys; tam tikri miego sutrikimai įeina į psichikos sutrikimų diagnostinius kriterijus.
2. Laiku atlikta miego sutrikimų diagnostika ir dėsningumų supratimas padeda pritaikyti individualias gydymo strategijas, pasiekti ilgalaikių teigiamų rezultatų, gydant psichikos ligas.
3. Psichikos sutrikimų gydymui taikomas farmakologinis gydymas reikšmingai veikia miegą. Išreikštą serotoninerginį ar noradrenerginį aktyvumą turintys antidepresantai sukelia nemigą, antihistamininių ar serotonino 5-HT2 receptorius blokuojančių savybių turintys antidepresantai didina mieguistumą, neuroleptikai pailgina miego trukmę, nuotaikos stabilizatoriai turi skirtingą poveikį – ličio druskos skatina lėtųjų bangų miegą, o antikonvulsantų poveikis miegui yra skirtingas.
4. Nefarmakologinės intervencijos, ypač kognityvinė elgesio terapija, skirta nemigai, miego higienos rekomendacijos, chronoterapija yra esminiai miego sutrikimų valdymo metodai. KET-N ne tik tiesiogiai pagerina miego kokybę, bet ir netiesiogiai sustiprina psichikos simptomų kontrolę, taip integruodamasi į biopsichosocialinio modelio pritaikymą gydant psichikos sutrikimus.